معلومات المنتج
|
اسم المنتج |
تحديد المنتج |
نموذج |
|
Click-iT EdU-488 مجموعة أدوات الكشف عن تكاثر الخلايا |
G1601 |
100T |
الوصف/المقدمة
يعد تحليل القدرة على تكاثر الخلايا طريقة تقييم شائعة ومهمة في علوم الحياة. ويمكنه الحكم على تأثير بعض الجينات والأدوية وما إلى ذلك على الخلايا المزروعة في المختبر، أو تحليل قدرة نمو وتجديد خلايا الأنسجة في ظل ظروف أو تحفيز مختلف. في الوقت الحاضر، هناك العديد من الطرق للكشف عن تكاثر الخلايا. يستخدم معظمها بعض الإنزيمات الأيضية التي تنتجها الخلايا لتقييم نشاط تكاثر الخلايا بشكل غير مباشر (مثل طريقة CCK-8 وطريقة MTT وما إلى ذلك)، ولكن بعض الأدوية أو حالة الخلية نفسها سيكون لها تأثير معين على نتائج التقييم. يُعرف الكشف المباشر عن تخليق الحمض النووي في الخلايا لتحديد تكاثر الخلايا باعتباره طريقة الكشف الأكثر دقة وفعالية. ومع ذلك، فإن كلاً من طريقة دمج النيوكليوسيدات الأصلية والتحسين اللاحق لطريقة BrdU بناءً على اكتشاف الأجسام المضادة لها حدودها الخاصة.
EdU (5-Ethynyl-2'-deoxyuridine، 5-ethynyl-2'-deoxyuridine) هو نظير الثيميدين الذي يحتوي على مجموعة الأسيتيلين، عندما يتم حقنه في الحيوانات أو الخلايا الحاضنة المستزرعة في في المختبر، يمكن لهذه الجزيئات الصغيرة أن تنتشر بسرعة إلى مختلف الأعضاء والأنسجة، وتتسلل إلى الخلايا، ويمكن أن تحل محل الثيميدين (T) في الحمض النووي المركب حديثًا أثناء تكاثر الخلايا. يمكن لمجموعة الأسيتيلين في جزيء EdU أن تتفاعل مع مسبار مركب الأزيد المسمى iF488 الفلورسنت لتشكيل حلقة تريازول مستقرة تحت تحفيز أيونات النحاس، لذلك يمكن تسمية الحمض النووي المركب حديثًا بمسبار الفلورسنت المقابل. بالمقارنة مع طريقة دمج النوكليوسيدات المشعة بالإشعاع، فإن طريقة الكشف عن EdU لا تحتوي على عوامل مقيدة مثل التلوث الإشعاعي؛ بالمقارنة مع طريقة الكشف عن BrdU، لا تتطلب طريقة الكشف عن EdU تمسخ الحمض النووي أو تفاعل الأجسام المضادة للمستضد، مما يقلل بشكل كبير من تعقيد التجربة ويجعل التجربة أيضًا أكثر توفيرًا للوقت وأكثر حساسية وأكثر استقرارًا وأكثر دقة.
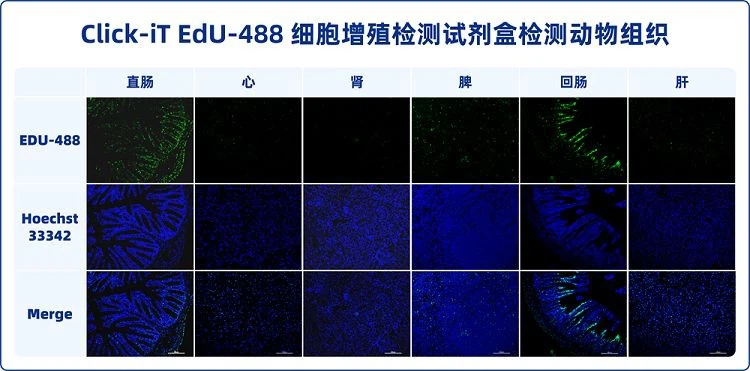
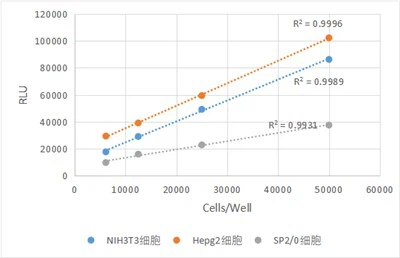
يمكن استخدام هذه المجموعة للكشف عن تكاثر الخلايا في الخلايا المستنبتة أو الأنسجة الحيوانية. مسبار الفلورسنت في هذه المجموعة هو مضان أخضر، والحد الأقصى لطول موجة الإثارة هو 491 نانومتر، والحد الأقصى لطول موجة الانبعاث هو 516 نانومتر. بعد تسمية الخلايا المتكاثرة، ستظهر نواة الخلية مضانًا أخضر ساطعًا، وسيتم تسمية نواة الخلية بشكل مشترك مع الصبغة النووية التقليدية المطابقة (توفر هذه المجموعة صبغة هويشت 33342 النووية للخلية)، يمكنك استخدام مجهر مضان، مجهر ليزر متحد البؤر وغيرها من الأدوات لمراقبة تكاثر الخلايا بشكل مباشر؛ يمكنك أيضًا استخدام قياس التدفق الخلوي للكشف عن شدة التألق للخلايا المستنبتة في المختبر، ثم تحديد دورة الخلية بناءً على نشاط تكرار الحمض النووي لكثافة التألق في مرحلة منتصف S.
شروط التخزين والمناولة
يجب تخزين الكاشف B (صبغة iF488) عند درجة -20 بعيدًا عن الضوء؛
يمكن تخزين الكاشف الحفاز EdU (الكاشف A) وعازل التفاعل عند درجة 4؛
صالحة لمدة 12 شهرا.
عناصر
|
رقم المكون |
عنصر |
G1601-100T |
|
G1601-1 |
محلول تخزين EdU (10 ملم) |
100 μL |
|
G1601-2 |
الكاشف أ |
120 μL |
|
G1601-3 |
الكاشف B (صبغة iF488) |
50 μL |
|
G1601-4 |
الكاشف ج |
2 × 100 ملغ (مسحوق) |
|
G1601-5 |
عازلة رد الفعل |
20 مل |
|
G1601-6 |
هويشت 33342 حل تلطيخ |
30 μL |
|
يدوي |
1 جهاز كمبيوتر |
|
ملاحظة: أوقات التفاعل المذكورة أعلاه مخصصة لفحص لوحة البئر 96-المقابلة.
تحضير التجربة
1. مستنبت الخلايا الذي يحتوي على المصل؛
2. حل النفاذية: 0.2-0.5% Triton X-100 في PBS (يوصي بمنتجنا، Cat.#:G1204)؛
3. المحلول المثبت: 4% بارافورمالدهيد في PBS، الرقم الهيدروجيني 7.4 (يوصي بمنتجنا،Cat.#:G1101)؛
4. المخزن المؤقت PBS (يوصي بمنتجنا، Cat.#:G4202)؛
5. الماء عالى النقاء.
6. الكواشف المتعلقة بالنمذجة الحيوانية وتقسيم الأنسجة (فحص تكاثر خلايا الأنسجة الحيوانية).
بروتوكول / إجراءات الفحص
1. المعالجة المسبقة للخلايا المزروعة في المختبر:
1.1. زرع الخلايا بالتساوي في لوحة ثقافة الخلية بكثافة معينة (يتم تحديد كثافة الزراعة بعوامل مثل حجم الخلية، وسرعة النمو، وما إلى ذلك). بعد أن تلتصق الخلايا بالجدار أو تعود إلى حالتها الطبيعية، قم بإجراء التحفيز الدوائي المقابل والعلاجات الأخرى. (بالنسبة للخلايا المعلقة، يرجى اتباع طريقة التشغيل العادية للخلايا المعلقة. تحتاج التجربة بأكملها إلى إضافة الطرد المركزي وخطوات أخرى).
1.2. تم طرد المادة المضافة الحفزية (الكاشف C) بسرعة منخفضة، وتم أخذ 100 مجم وإذابتها بإضافة 1 مل من الماء عالى النقاء وتوزيعها وتخزينها عند درجة -20، وتم الاحتفاظ بالمسحوق المتبقي كاحتياطي.
2. وضع العلامات على EdU الخلوية في المختبر، والتثبيت والنفاذية:
2.1. إعداد 2 × EdU حل عمل الحضانة: أضف 2 ميكرولتر من محلول تخزين EdU (10 مم) إلى كل 1 مل من وسط زراعة الخلايا الكاملة، وهو 20 ميكرومتر 2 × EdU حل عمل الحضانة، ووضعه في الحاضنة للتسخين المسبق (الموصى به) تركيز العمل إيدو هو 10 ميكرومتر للتجارب الأولية)؛
2.2. في وضع نصف التغيير، نضح نصف مستنبت الخلية الأصلي في لوحة الاستنبات، وأضف حجمًا متساويًا من محلول عمل الحضانة المسخن مسبقًا 2 × EdU، واحتضنه لفترة معينة من الزمن (تعتمد مدة الحضانة عمومًا على دورة نمو الخلايا المقابلة، والتي تمثل عادة حوالي 10٪ من دورة الخلية بالنسبة للخلايا الملتصقة وسريعة النمو في الغالب، يوصى بالحضانة لمدة 2 ساعة في حالات محددة، يجب تعديلها مع خصائص الخلية، والوضع الفعلي بعد العلاج، وما إلى ذلك. إذا كان هناك حاجة إلى فترة حضانة أطول، يمكن تقليل تركيز عمل EdU بشكل مناسب لفترة أقصر، ويمكن زيادة تركيز EdU بشكل مناسب)؛
2.3. بعد حضانة EdU، اغسل باستخدام المخزن المؤقت PBS لمدة 1-2 مرات، وأضف سائل التثبيت لتغطية الخلايا، ثم ثبته في درجة حرارة الغرفة لمدة 15 دقيقة (إذا كان قياس التدفق الخلوي مطلوبًا، يجب هضم الخلايا الملتصقة وإعادة تعليقها قبل هذه الخطوة إصلاح، اتبع طريقة معالجة خلية التعليق)؛ اغسل 2-3 مرات باستخدام المخزن المؤقت PBS، 3-5 دقيقة في كل مرة؛
2.4. إزالة المخزن المؤقت لبرنامج تلفزيوني، وإضافة الحل بيرميبيليزيشن لتغطية الخلايا، واحتضان في درجة حرارة الغرفة لمدة 15 دقيقة؛
2.5. قم بإزالة محلول النفاذية، واغسل 1-2 مرات باستخدام المخزن المؤقت PBS، 3-5 دقيقة في كل مرة. ثم انتقل إلى الخطوة 4.
3. نمذجة حقن الحيوانات EdU وكذلك معالجة قسم الأنسجة:
3.1. وفقا للمتطلبات التجريبية، يتم استخدام حقنة واحدة أو أكثر من إيدو لنموذج الحيوانات عن طريق الحقن داخل الصفاق، والحقن العضلي، والحقن تحت الجلد، وحقن الوريد الذيل، وما إلى ذلك. وبشكل عام، فإن نسبة جرعة إيدو إلى وزن جسم الحيوان هي 5 ملغم / كغم، الفعلية تعتمد جرعة الحقن على محتوى البحث وظروف الحيوان. يتم استخدام حل تخزين EdU المتوفر في هذه المجموعة بشكل أساسي لوضع العلامات على الخلايا المختبرية EdU. إذا كنت بحاجة إلى نموذج حيوان مع EdU، يمكنك طلب كاشف EdU بشكل منفصل (القطة رقم: G5059)؛
3.2. تتكاثر الخلايا الظهارية مثل الأمعاء الدقيقة بسرعة، بينما تتكاثر خلايا الدماغ ببطء. عادة ما تستغرق الأنسجة سريعة النمو أقل من 12 ساعة لوضع العلامات، بينما قد تستغرق الأنسجة بطيئة النمو عدة أيام لوضع العلامات. تم تحديد الوقت الأمثل لوضع العلامات وفقًا للتجربة المحددة. ونظرا للانتشار السريع للأنسجة الظهارية المعوية، أوصى بهذه الأنسجة كمرجع لوضع العلامات.
3.3. بعد ذبح الحيوان حسب المعايير المحددة يتم إخراج الأنسجة اللازمة وعمل المقاطع المجمدة أو المقاطع البارافينية حسب الإجراءات التقليدية:
أ. بالنسبة للأجزاء المجمدة: أعيدي المقاطع إلى درجة حرارة الغرفة، وأضيفي كمية مناسبة من سائل التثبيت، وثبتيها في درجة حرارة الغرفة لمدة 15 دقيقة. قم بإزالة سائل التثبيت واغسله 3 مرات باستخدام محلول PBS المؤقت لمدة 3-5 دقيقة لكل منهما؛ إزالة المخزن المؤقت لبرنامج تلفزيوني وتغطية الأنسجة بكمية مناسبة من محلول النفاذية واحتضانها في درجة حرارة الغرفة لمدة 10-15 دقيقة؛ إزالة الحل permeabilization ويغسل مع PBS المخزن المؤقت 1- 2 مرات، 3-5 دقيقة في كل مرة. ثم انتقل إلى الخطوة 4.
ب. بالنسبة لأقسام البارافين: قم بإزالة البارافين وترطيب المقاطع، واغسلها باستخدام برنامج تلفزيوني لمدة 5 دقائق. إزالة المخزن المؤقت لبرنامج تلفزيوني وإضافة الحل بيرميبيليزيشن لتغطية الخلايا أو الأنسجة، واحتضان في درجة حرارة الغرفة لمدة 15 دقيقة؛ ثم يغسل مع المخزن المؤقت لبرنامج تلفزيوني لمدة 1-2 مرات، في كل مرة لمدة 3-5 دقيقة. ثم انتقل إلى الخطوة 4.
4. رد فعل النقر فوق EdU:
4.1. أثناء تثبيت الخلايا أو الأنسجة وثقبها، تحضير محلول التفاعل: قم بخلط الكواشف وفقًا للنسبة التالية، يمكن زيادة أو تقليل حجم المستحضر بما يتناسب مع عدد العينات.
|
عنصر |
الحجم (للخلية) |
الحجم (للقسم النسيجي) |
|
عازلة رد الفعل |
935 μL |
928 μL |
|
الكاشف أ |
10 μL |
10 μL |
|
الكاشف B (صبغة iF488) |
5 μL |
12 μL |
|
الكاشف ج |
50 μL |
50 μL |
|
القدرة الإجمالية |
1000 μL |
1000 μL |
4.2. إزالة المخزن المؤقت لبرنامج تلفزيوني من الخلايا أو الأقسام، وإضافة محلول التفاعل، ويهز بلطف للتأكد من أن محلول التفاعل يغطي جميع الخلايا أو الأنسجة، واحتضان لمدة 30 دقيقة في درجة حرارة الغرفة في الظلام؛
4.3. قم بإزالة محلول التفاعل، واغسل 2-3 مرات باستخدام المخزن المؤقت PBS، 3-5 دقيقة في كل مرة (إذا لم يكن هناك متطلبات خاصة أخرى، يمكن اكتشاف شدة التألق عن طريق قياس التدفق الخلوي أو يمكن اكتشاف تأثير التألق بواسطة أدوات أخرى).
5. وصمة عار النووية (اختياري):
5.1. تمييع حل تلطيخ هويشت 33342 مع المخزن المؤقت لبرنامج تلفزيوني بنسبة 1: 500-1000، وإضافة إلى العينة لتغطية الخلايا، واحتضان لمدة 5 دقائق؛
5.2. قم بإزالة محلول تلطيخ Hoechst 33342، واغسل 2-3 مرات باستخدام المخزن المؤقت PBS، 3-5 دقيقة في كل مرة.
6. تحليل التصوير والكشف:
استخدم المجهر الفلوري أو المجهر البؤري للكشف عن الخلايا المعالجة أو عينات قسم الأنسجة، وتحليل نسبة الخلايا المتكاثرة. وبدلاً من ذلك، يمكن جمع الخلايا المستزرعة في المختبر ويمكن قياس شدة التألق عن طريق قياس التدفق الخلوي (يوصى باستخدام عينات الخلايا غير المسماة بـ EdU كعنصر تحكم سلبي لفحص قياس التدفق الخلوي واختيار الجهد المناسب)، وعلى أساس على شدة التألق، يمكن تحديد نشاط تكرار الحمض النووي للمرحلة S في دورة الخلية. تتوافق صبغة الفلورسنت iF488 (الكاشف B) في هذه المجموعة مع التوصيف الطيفي لـ Ex/Em: 491 نانومتر/516 نانومتر (أخضر)؛ يتوافق محلول تلطيخ Hoechst 33342 مع التوصيف الطيفي لـ Ex/Em: 346 نانومتر/460 نانومتر (أزرق).
ملحوظة
1. بالنسبة للخلايا المستنبتة، يمكن تعديل تركيز EdU المحدد ووقت الحضانة بشكل مناسب اعتمادًا على العينة والغرض البحثي.
2. تتكاثر بعض خلايا الأنسجة ببطء. من أجل تجنب تأثير النمذجة الضعيفة، يوصى باختيار عينات الأنسجة ذات الانتشار السريع كعينات مرجعية (مثل الأنسجة المعوية).
3. إذا كان لون الخلفية غامقًا جدًا، فقد يكون سبب ذلك عدم كفاية الغسيل، أو التثبيت لفترة طويلة، أو المثبت المتبقي، وما إلى ذلك في التجربة.
4. الكاشف C (كاشف الإضافة الحفزية EdU) سهل الأكسدة. حاول تجنب التعرض لفترات طويلة للهواء. بعد تحضيره كمحلول مائي، يوصى بتخزينه في قسامة؛ تم اختباره، مثل تغيير لون الكاشف الإضافي التحفيزي EdU قليلاً، ولا يزال النظام التحفيزي لتفاعل النقر قادرًا على المضي قدمًا بشكل طبيعي. إذا ظهر الكاشف C باللون البني، فهذا يشير إلى انتهاء صلاحية المكون، لذا يرجى التخلص منه.
5. من أجل صحتك وسلامتك، يرجى ارتداء معاطف وقفازات المختبر أثناء العملية.
للاستخدام البحثي فقط!
الوسم : مجموعة أدوات اكتشاف انتشار الخلايا click-it edu-488، الصين مجموعة أدوات اكتشاف انتشار الخلايا click-it edu-488 الشركات المصنعة والموردين والمصنع